骨髓增生異常綜合征(MDS)是一種克隆性血液係統惡性腫瘤,由具有體細胞突變的異常造血幹細胞(HSCs)引起,以分化障礙、外周血細胞減少和易患急性髓係白血病(AML)為特征。與AML細胞不同,MDS克隆的生長速度通常低於正常造血幹細胞,這是因為MDS啟動細胞在小鼠MDS模型中表現出競爭劣勢。 矛盾的是,MDS克隆並沒有被根除,並在長時間的潛伏期後逐漸在骨髓(BM)中與正常的HSCs競爭。為了解釋這
骨髓增生異常綜合征(MDS)是一種克隆性血液係統惡性腫瘤,由具有體細胞突變的異常造血幹細胞(HSCs)引起,以分化障礙、外周血細胞減少和易患急性髓係白血病(AML)為特征。與AML細胞不同,MDS克隆的生長速度通常低於正常造血幹細胞,這是因為MDS啟動細胞在小鼠MDS模型中表現出競爭劣勢。
矛盾的是,MDS克隆並沒有被根除,並在長時間的潛伏期後逐漸在骨髓(BM)中與正常的HSCs競爭。為了解釋這些相互矛盾的發現,有必要考慮BM微環境和HSCs之間的相互作用。

圖片來源:https://doi.org/10.1016/j.celrep.2022.110805
近日,東京大學的研究者們在“Cell Report”雜誌上發表了題為“MDS cells impair osteolineage differentiation of MSCs via extracellular vesicles to suppress normal hematopoiesis”的文章,該研究揭示了新的MDS EV-MSC軸在無效造血中的作用。
骨髓增生異常綜合征(MDS)是一種造血幹細胞(HSCs)的克隆性疾病,以無效造血和頻繁進展為白血病為特征。MDS細胞的增殖能力較弱,它如何抑製正常的造血並最終主導骨髓空間,長期以來一直沒有解決。盡管有幾項研究表明間充質基質或幹細胞(MSCs)在抑製正常造血中起作用,但這一過程背後的分子機製仍不清楚。
在這裏,研究者證明了人和小鼠的MDS細胞都通過抑製MSCs的骨線分化來擾亂骨代謝,從而削弱了MSCs支持正常HSCs的能力。增強的MSC分化挽救了體內和體外MDS模型中被抑製的正常造血。有趣的是,這種抑製效應是可逆的,並由來自MDS細胞的細胞外小泡(EVS)介導。
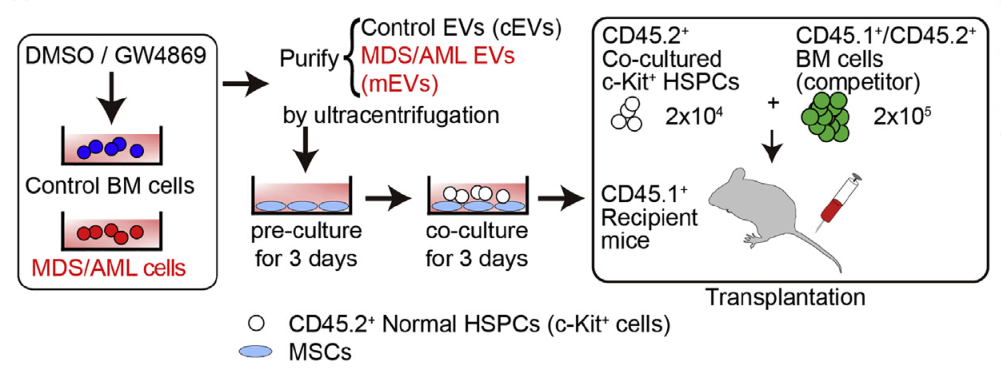
MDS/AML細胞EV對MSCs功能的幹擾
圖片來源:https://doi.org/10.1016/j.celrep.2022.110805
綜上所述,該研究證明MSCs向骨線樣細胞分化的障礙在MDS的骨髓衰竭中起著關鍵作用,並且MDS的有效治療需要去除MDS細胞,同時恢複支持的小生境。該研究還表明,MEVS導致MSCs功能障礙,導致正常造血抑製。這些發現表明,MEVS調控的生物過程是MDS有吸引力的治療靶點。(生物穀Bioon.com)
參考文獻
Yasutaka Hayashi et al. MDS cells impair osteolineage differentiation of MSCs via extracellular vesicles to suppress normal hematopoiesis. Cell Rep. 2022 May 10;39(6):110805. doi: 10.1016/j.celrep.2022.110805.
版權聲明 本網站所有注明“來源:生物穀”或“來源:bioon”的文字、
copyright©醫學論壇網 版權所有,未經許可不得複製、轉載或鏡像
京ICP證120392號 京公網安備110105007198 京ICP備10215607號-1 (京)網藥械信息備字(2022)第00160號