線粒體是細胞代謝,天然免疫和細胞凋亡控製中心,其功能遠遠超出了人們傳統的認知細胞的能量工廠。線粒體廣泛參與眾多細胞生物學過程包括細胞的命運決定和衰老。因此,線粒體需要精細的、多層次的質量監控係統來保障其正常功能。進化上高度保守的線粒體蛋白酶是線粒體質量控製的第一道防線,然而既往的研究絕大多數集中於線粒體生物生成、分裂/融合與自噬等,對於線粒體蛋白穩態控製的作用機製和生理意義卻十分不清楚。 除了介
線粒體是細胞代謝,天然免疫和細胞凋亡控製中心,其功能遠遠超出了人們傳統的認知—細胞的能量工廠。線粒體廣泛參與眾多細胞生物學過程包括細胞的命運決定和衰老。因此,線粒體需要精細的、多層次的質量監控係統來保障其正常功能。進化上高度保守的線粒體蛋白酶是線粒體質量控製的第一道防線,然而既往的研究絕大多數集中於線粒體生物生成、分裂/融合與自噬等,對於線粒體蛋白穩態控製的作用機製和生理意義卻十分不清楚。
除了介導錯誤折疊或受損蛋白質的降解作用外,近年來研究還發現線粒體蛋白酶還通過執行高度調節的蛋白水解反應來調控線粒體功能,是線粒體可塑性調節的關鍵一環。人類線粒體蛋白酶的失活突變可導致多種遺傳性疾病,並且在許多病理狀態下(例如神經退行性疾病、代謝綜合征和癌症)也觀察到線粒體蛋白酶水解活性的降低。然而,人們對於線粒體蛋白穩態是否與細胞命運決定和衰老有內在關聯仍然未知。
2023年5月22日,南京大學甘振繼課題組聯合中國科學院微生物、發育與健康研究中心邵孟樂課題組在 Nature Cell Biology 期刊發表了題為:Proteolytic rewiring of mitochondria by LONP1 directs cell identity switching of adipocytes 的研究長文。
該研究發現了依賴蛋白酶LONP1的線粒體蛋白水解重排調控白色脂肪細胞的命運轉變;揭示了高度調控的線粒體蛋白酶是細胞的關鍵感應紐帶,將細胞外環境刺激、線粒體呼吸鏈複合物/代謝重排與白色脂肪產熱重塑過程中的細胞命運重編程有機聯係起來。

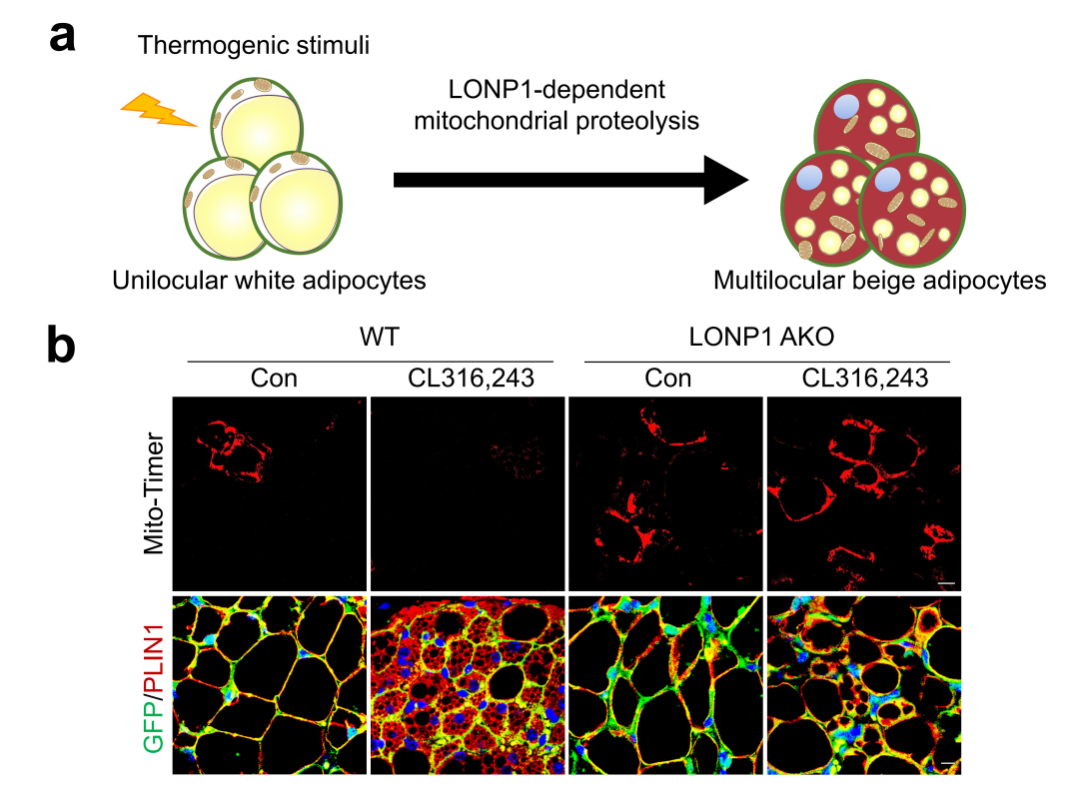
儲存能量的白色脂肪細胞向燃燒能量的米色脂肪細胞的細胞命運轉變是哺乳動物免受寒冷環境中體溫過低的關鍵機製。這一脂肪細胞命運轉變能力的降低導致機體適應性產熱能力減退是衰老的重要標誌之一。低溫或b3-腎上腺素激動劑刺激可誘導單室大脂滴形態的白色脂肪細胞進行劇烈的細胞重編程過程,轉變成多室小脂滴形態的米色脂肪細胞,這一進程又被稱為“米色化”或“褐脂化”,其一大特征就是線粒體數量和活性大量增加以滿足細胞產熱的需求。
除了線粒體生物生成外,白色脂肪細胞米色化還伴隨著線粒體蛋白質組的深刻變化,以滿足線粒體呼吸與能量代謝激增的要求。解偶聯蛋白1(UCP1)的急劇增加就是一個很好的例子,UCP1是一種線粒體內膜轉運蛋白,能通過消散電化學質子梯度將細胞呼吸與ATP產生解偶聯。因此,保障線粒體內蛋白質組的功能及其應對產熱刺激的可塑性對於脂肪細胞的命運轉變至關重要。
此前,甘振繼教授課題組係列研究發現了線粒體蛋白穩態控製在調節骨骼肌代謝穩態中起著至關重要的作用,並揭示了肌肉線粒體蛋白穩態應激可長程調控白色脂肪組織產熱重塑(Xu et al,Nat Commun. 2022;Guo et al, Sci Adv. 2022)。
在此研究基礎上,該課題組綜合應用遺傳學、生物物理和生物化學等方法,進一步探究了線粒體蛋白穩態控製係統對脂肪細胞命運轉變的潛在調節功能。首先,通過 Mito-Timer 轉基因小鼠及硫醇探針Tetraphenylethene maleimide(TPE-MI),作者可視化展示並定量揭示了產熱刺激可特異性增強白色脂肪細胞中依賴蛋白酶LONP1的蛋白水解動態調節規律。通過係列脂肪細胞特異性 LONP1功能缺失細胞和小鼠模型,發現盡管成熟白色脂肪細胞僅含有少量的線粒體,但依賴LONP1控製的線粒體蛋白穩態是白色脂肪細胞米色化的先決條件(圖1)。得益於“AdipoChaser”遺傳譜係追蹤係統,研究者揭示了LONP1的失活顯著削弱成熟白色脂肪細胞向米色脂肪細胞的命運轉變(圖1)。
緊接著,基於TurboID的鄰近標記技術被用來尋找LONP1蛋白水解的底物。通過融合應用了定量代謝組學方法對LONP1缺陷型或野生型米色脂肪細胞進行係統代謝物比較分析,研究者發現並證明了脂肪細胞命運決定的全新機製:即LONP1通過特異性調節線粒體呼吸鏈複合物II關鍵組分SDHB的降解,來確保足夠量的胞內琥珀酸水平,從而保障白色脂肪細胞向米色脂肪細胞的命運轉變。進一步經過細胞生化和染色質免疫沉澱和測序分析,發現受LONP1調節的脂肪細胞內琥珀酸與α-酮戊二酸(α-KG)的比例變化引發產熱基因的組蛋白甲基化狀態改變,從而調控白色脂肪細胞向米色脂肪細胞轉變的基因重編程。最後,研究者還發現在年老小鼠脂肪細胞中重新激活LONP1-琥珀酸通路可以恢複老年白色脂肪細胞向米色脂肪細胞轉變的能力,並挽救老年小鼠適應性產熱能力的下降。
該研究發現了高度調控的線粒體蛋白水解重排控製細胞命運決定;拓展了人們對特異性線粒體蛋白降解及其引發線粒體呼吸鏈複合物/代謝重塑的重要調節功能和生理意義的認識;揭示了白色脂肪細胞內琥珀酸作為細胞命運信使新的重要功能—超越其作為線粒體氧化代謝底物的作用;提出了通過修複線粒體蛋白穩態來治療與脂肪衰老相關的代謝紊亂的一種新策略。
值得一提的是,Nature Cell Biology 邀請該文的通訊作者在同期發表了題為:Mitoprotease LONP1 controls white-to-beige adipocyte conversion via metabolic enzyme turnover 的Research Briefing文章,研究者針對線粒體蛋白穩態控製和線粒體代謝物調控細胞命運轉變方向提出了未來研究的多個重要科學問題。
Nature Cell Biology 還邀請領域內專家,美國HHMI,猶他大學的 Jared Rutter 教授點評了該項研究成果,他認為該工作回答了線粒體蛋白酶在白色脂肪組織重塑中的作用這一懸而未決的問題。開啟了靶向脂肪褐色化和能量平衡的新藥物治療可能……”。期刊資深編輯 Melina Casadio 博士也高度評價該項成果“Unlike the ‘textbook’ view of mitochondrial metabolism and ETC organization”,認為不同於傳統“教科書”觀點,該項研究揭示了細胞會通過調控線粒體ETC來適應其代謝需求。
南京大學副研究員付婷婷,博士研究生孫婉平,碩士研究生薛嘉宸和博士研究生周正為論文共同第一作者,南京大學甘振繼教授和中國科學院微生物、發育與健康研究中心邵孟樂研究員為論文共同通訊作者。共同作者裏還有大連化物所的樸海龍教授,美國西南醫學中心的Philipp E. Scherer教授,南華大學的呂斌教授,南京大學的方雷、朱敏生、陳韻聰教授等。研究得到合作實驗室的大力協助與支持。
原始出處:
Fu, T., Sun, W., Xue, J. et al.Proteolytic rewiring of mitochondria by LONP1 directs cell identity switching of adipocytes. Nat Cell Biol (2023). https://doi.org/10.1038/s41556-023-01155-3.
copyright©醫學論壇網 版權所有,未經許可不得複製、轉載或鏡像
京ICP證120392號 京公網安備110105007198 京ICP備10215607號-1 (京)網藥械信息備字(2022)第00160號