房間裏逐漸蓄積的代謝物二氧化碳(CO2)是我們工作效率低下的元凶。
北有暖氣南有空調,即使窗外大雪紛飛,室內依舊溫暖如春,但房間裏逐漸蓄積的代謝物二氧化碳(CO2)是我們工作效率低下的元凶。擁擠的辦公室中的CO2濃度易高於1%,人會感到煩躁和心悸;密閉臥室中一晚蓄積的CO2濃度常高於2%,人會感到氣喘、焦慮、睡不醒。實際上,空氣中CO2含量僅為0.03%,在我們所處的環境中卻高出幾百倍!
焦慮和氣喘是血管對高濃度CO2作出的自我保護機製,提示環境可能有潛在的危險;而這種腦血管響應性的喪失將導致一係列呼吸係統疾病和焦慮症的產生。
加州大學的Markus Schwaninger課題組近日在PNAS上發表工作,發現腦血管響應高濃度CO2點關鍵蛋白和通路,闡明了CO2引起特定呼吸模式和焦慮的機製。
CO2在血液緩衝體係中被迅速轉化為氫離子和碳酸。CO2的許多生理效應都由氫離子介導,例如呼吸刺激和恐懼反應,並且氫離子能引起強烈的血管擴張而導致大腦灌注增加。這一現象的產生與G蛋白偶聯受體有關,僅GPR4 和GPR68兩種G蛋白表達在血管中。
因此研究者構建了這兩種G蛋白基因敲除的動物,將其分別暴露在10%CO2環境中,發現CO2引發的前腦初代血管擴張效應在GPR4-KO小鼠中減弱了。CO2感受器應位於內皮細胞中,而原位雜交驗證發現GPR68表達在血管平滑肌上,因此說明GPR4才是腦血管內皮細胞中響應CO2的關鍵蛋白。
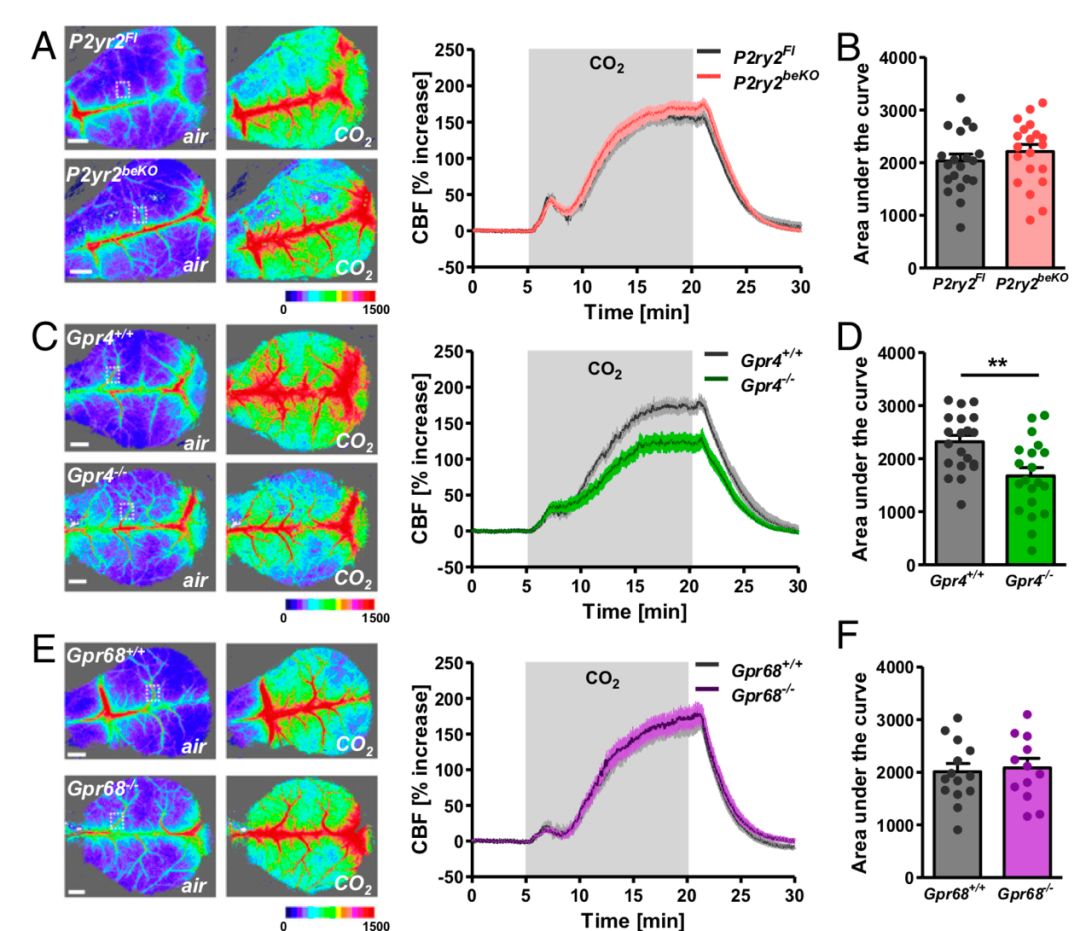
GPR4是腦血管中感受CO2的關鍵蛋白
進一步,研究者通過Gαq/11抑製劑,證明CO2/H+作用於內皮細胞的氫離子感受器GPR4 ,進而激活下遊的Gαq/11蛋白以增加前列環素和一氧化氮的釋放,從而促進腦血管的擴張。
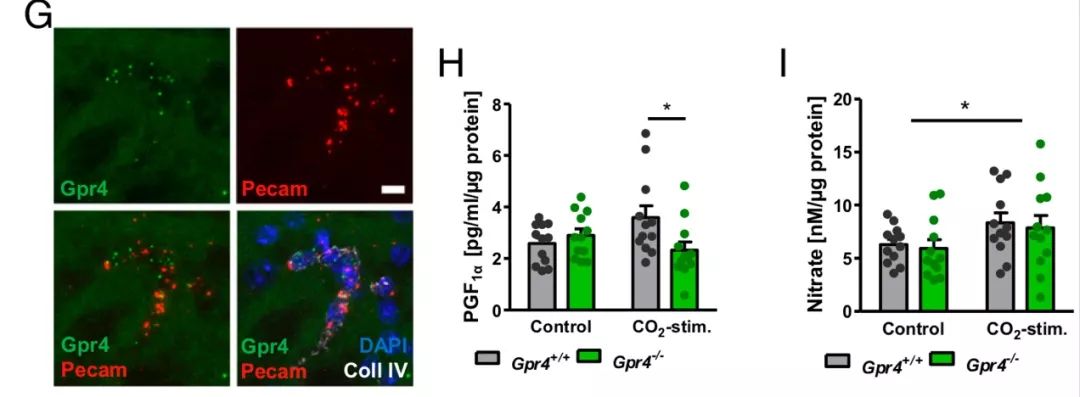
GPR4促進前列環素和一氧化氮釋放
接下來,研究者們發現GPR4蛋白缺失後,腦血管對CO2的響應嚴重失常。正常小鼠暴露在高濃度CO2下,用MRI核磁共振能檢測到腦灌注增加,離體腦片皮層的血管直徑增加,但GPR4-KO小鼠則不會發生以上響應。
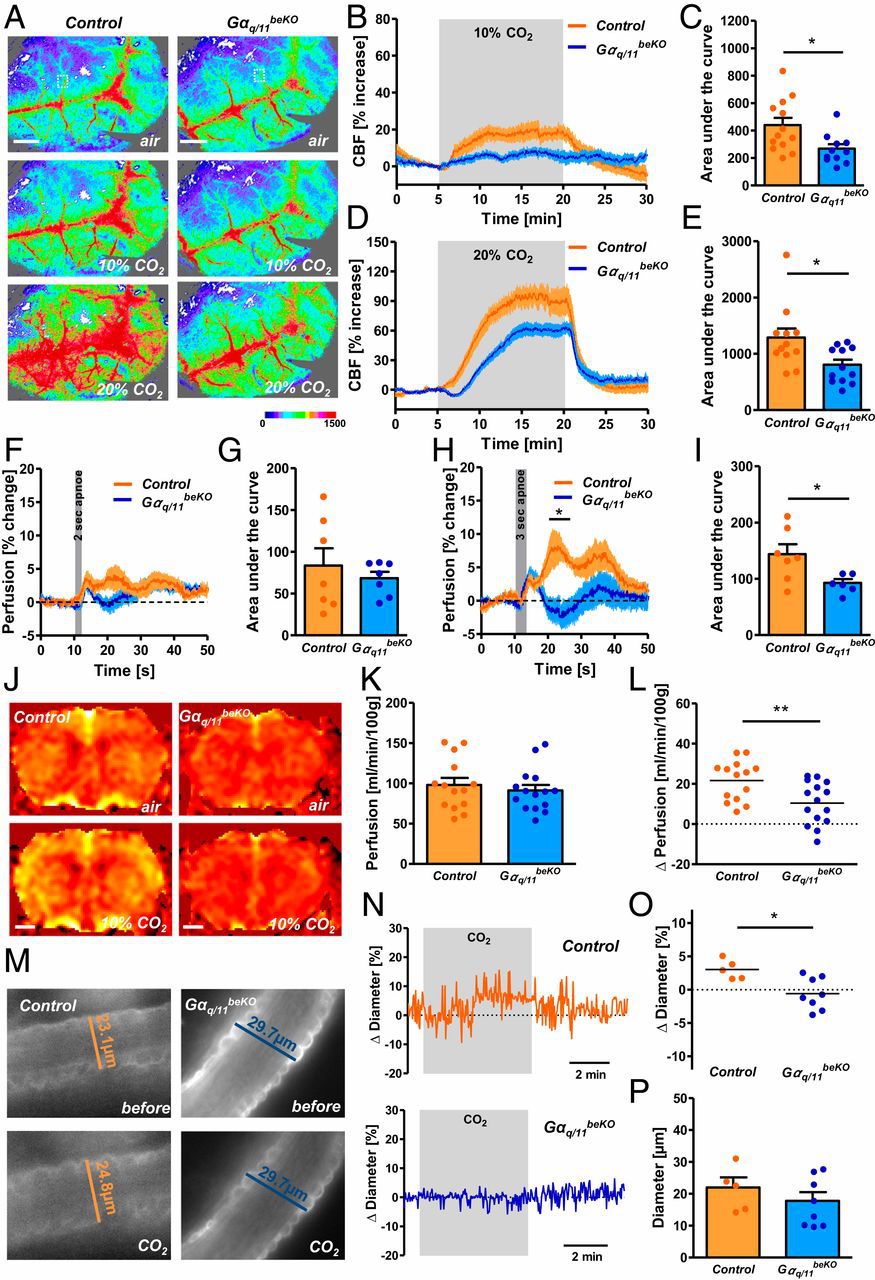
GPR4蛋白缺失導致腦血管對CO2的響應失常
當體內CO2濃度升高時,身體會發出窒息的預警,例如緊張不安、焦躁煩悶。前期在人類和齧齒類中的研究表明,高濃度CO2會激活大腦中主宰恐懼和驚慌的腦區——基底前腦杏仁核。
研究者發現,暴露在高濃度CO2環境中的對照組杏仁核灌注增加,而GPR4-KO小鼠無明顯變化。在高濃度CO2環境或正常環境下,GPR4-KO小鼠均表現出更多的“驚呆”行為,說明其始終表現出更高的恐懼反應;GPR4-KO小鼠在曠場實驗中貼壁運動更多,在高架十字迷宮的開臂中運動時間更短,更傾向於待在安全範圍內而不對陌生環境進行探索,說明GPR4蛋白的缺失增加小鼠基礎狀態下的焦慮反應。
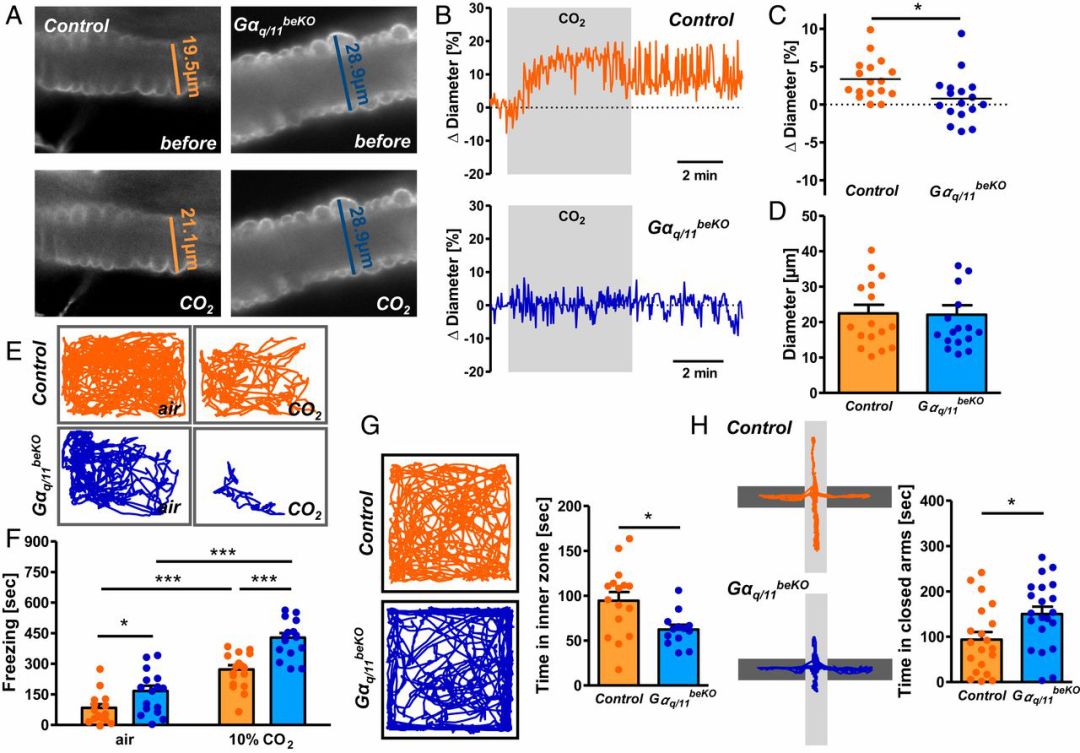
GPR4蛋白缺失使小鼠更焦慮
(圖G曠場實驗,小鼠在空曠新環境中運動到中心區域代表探索行為,緊貼牆壁代表緊張焦慮:圖H高架十字迷宮實驗,在高處的交叉通道,僅黑色通道(閉臂)有圍欄,通過統計小鼠到開臂上探索的時間,評價其焦慮水平。圖中顯示小鼠的運動軌跡。)
二氧化碳作用於腦幹不同區域增加呼吸頻率和潮氣量。研究者發現腦幹的梯形後核(RTN)有GPR4表達。與皮層和杏仁核的灌注結果相反,高濃度CO2環境引起正常小鼠的RTN血管收縮,刺激呼吸反應增強,並重啟類似窒息的呼吸暫停;而GPR4-KO小鼠呼吸減弱,呼吸暫停時間延長。腦血管反應性受損會使患者易產生呼吸暫停發作,這與糖尿病或肥胖症等疾病的呼吸並發症相似。
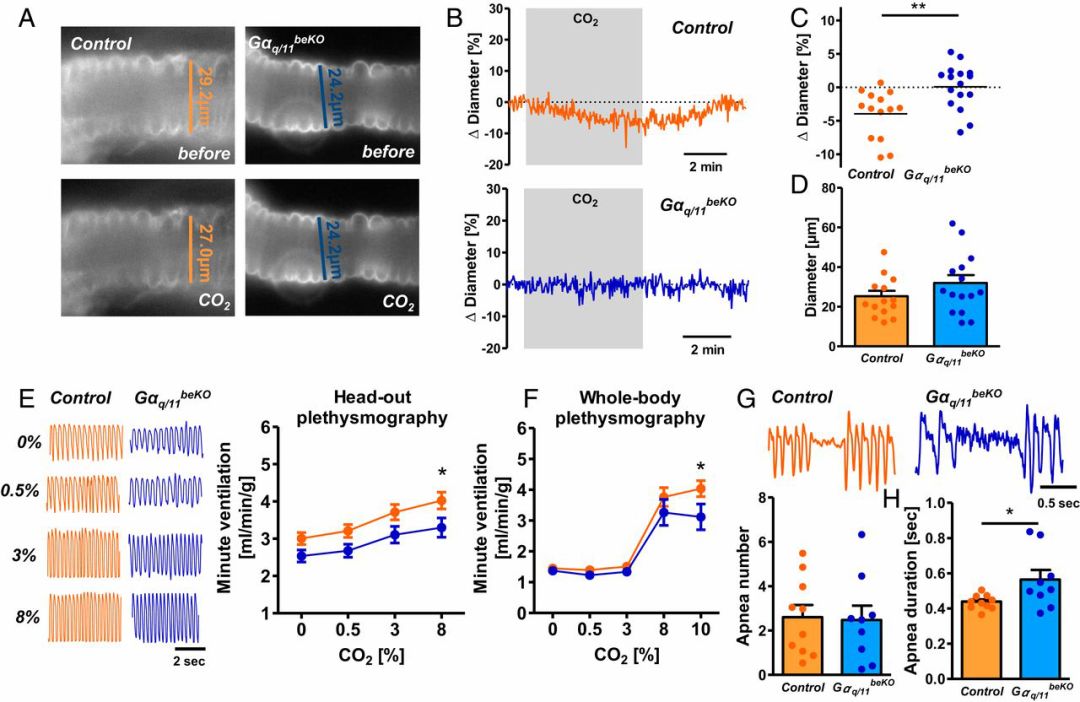
GPR4蛋白缺失使小鼠對高濃度CO2環境呼吸代償紊亂
這項研究闡明了腦血管的二氧化碳反應性是由關鍵蛋白GPR4介導並激活下遊Gαq/11所產生的,在不同腦區產生的作用效應不同,引發了高濃度二氧化碳下的焦慮和特殊呼吸模式。GPR4蛋白功能受損導致的腦血管反應性減弱,是內皮功能障礙診斷的關鍵特征,有望作為睡眠呼吸暫停、焦慮症和相關的代謝綜合征並發症等治療新靶標!
copyright©醫學論壇網 版權所有,未經許可不得複製、轉載或鏡像
京ICP證120392號 京公網安備110105007198 京ICP備10215607號-1 (京)網藥械信息備字(2022)第00160號